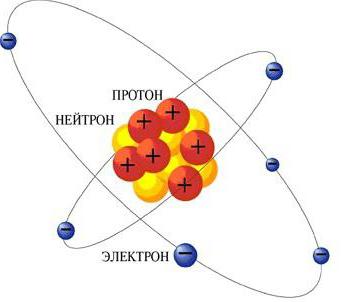
Електронна конфигурация - тайните на структурата на атома
През есента на 1910 г., Ернст Ръдърфорд,meditating, се опита да разбере вътрешната структура на атома. Неговите експерименти върху разпръскването на алфа частици от различни вещества убедително доказани - вътре в атома има някакво масивно тяло, което досега не е преценено. През 1912 г. Ръдърфорд ще го нарече атомно ядро. В главата на учения хиляди въпроси се надигнаха. Каква е натовареността на това неизвестно тяло? Колко електрони са необходими, за да се гарантира теглото му?

През май 1911 г. Ръдърфорд публикува статияатомната структура, която предшества много важно предупреждение, че стабилността на атомната структура може да зависи от тънкостите на вътрешната структура на атома и движението на заредени частици, които са му основен структурен компонент. Така се роди електронната конфигурация - атомният ядрен електронен модел. Този модел е предназначен да играе безценна роля в ядрената физика.

Електронната конфигурация е редътразпределението на електроните в атомните орбити. Благодарение на любознателен ум и постоянство Ърнест Ръдърфорд, който е в състояние да защити идеята си, науката е обогатен с нови знания, значението на които не може да се надценява.
Електронната конфигурация на атома е както следва. В центъра на цялата структура е ядрото, състоящо се от различен брой неутрони и протони за всяко вещество. Това, което определя положителния заряд на ядрото. Около него в съответните концентрични орбити се движат електрони - отрицателно заредени елементарни частици. Тези атомни орбити също се наричат черупки. Външната орбита на атома се нарича валентност. И броят на електроните върху него е валентност.
Всяка електронна конфигурация на елементитеразличен брой електрони, съдържаща се в него. Например, много просто въпрос на свят - водород - съдържащ само един електрон, кислороден атом, - осем и електронно конфигурация желязо има двадесет и шест електрони.
Но определящата стойност в електронния моделатомът изобщо не разполага с броя на електроните, но това, което ги държи заедно и прави цялата система правилно функционира - ядрото и неговият състав. Това е ядрото, което придава на веществото неговите индивидуални качества и характеристики. Електроните понякога напускат атомния модел, а след това атомът придобива положителен заряд (благодарение на ядрения заряд). В този случай веществото не променя свойствата си. Но ако промените състава на ядрото, то ще бъде напълно различно вещество с различни качества. Това не е лесно, но все още е възможно.
Тъй като електронната конфигурация е невъзможна безнеговият основен структурен елемент - атомното ядро, трябва да обърне специално внимание. Това е централният елемент на атомния модел, който формира индивидуалните свойства и характеристики на всяко химично вещество. Протоните, които в действителност дават на ядрото положителен заряд, са 1840 пъти по-тежки от всеки електронен. Но силата на заряда на протона е равна на тази на всеки електронен. В състояние на равновесие броят на протоните в един атом е равен на броя на електроните. В този случай ядрото е носител на нулевия заряд.
Друга важна част от атомното ядро се нарича неутрон. Този елемент няма такса, която е направила верижна ядрена реакция възможна. Така че е просто невъзможно да надценяваме стойността на неутрона.