Алифатни въглеводороди са какво?
Алифатни въглеводороди са органични съединения, чиито молекули съдържат само единична връзка. Те включват алкани и циклопарафини, техните характеристики ще бъдат разгледани в нашия материал.
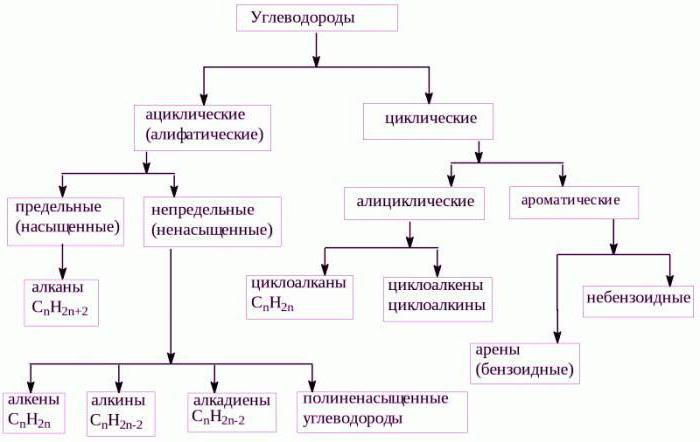
Общата формула на алканите
Представители на този клас се характеризират сс обща формула CnH2n + 2. Парафините включват всички съединения с отворена верига, където атомите са свързани заедно чрез прости връзки. Поради факта, че при нормални условия, алифатните въглеводороди са слабо активни съединения, те се наричат "парафини". Ще изясним някои характеристики на структурата на представителите на този клас, естеството на връзката в молекулите, областта на приложение.

Кратко описание на метана
Като най-прост представител на този клас, можем да споменем метан. Той е, който започва алифатната серия от въглеводороди. Разкриваме неговите отличителни черти.
Метанът е в нормални условиягазово вещество, което е без мирис и безцветно. Това съединение се образува в природата чрез разлагане без наличието на кислород на въздух от животни и растителни организми. Например, той се намира в природния газ, така че в момента той се използва в големи количества като гориво в производството и в ежедневието.
Какъв вид химична връзка имат тези въглеводороди? Алифатни, ограничаващи органични съединения са ковалентни полярни молекули.
Молекулата на метана има тетраедна формамолекула, вида на хибридизация на въглеродни атоми в него sp3, което съответства на ъгъл на валентност от 109 градуса 28 минути. По тази причина алифатните въглеводороди са химически слабо активни съединения.

Характеристики на метан хомолози
В допълнение към метана в природен газ и нефт,Други въглеводороди, които имат подобна структура с него. Първите четирима представители на хомоложната серия парафини са в газообразно агрегатно състояние, имат незначителна разтворимост във вода.
Като роднинаУвеличаването на точките на кипене и точката на топене на CdHy се наблюдава в молекулната маса. Между отделните представители на поредицата има определена разлика CH2, която се нарича хомоложна разлика. Това е пряко потвърждение за принадлежността на съединението към тази органична серия.
Всички алифатни въглеводороди са вещества, които са лесно разтворими в органични разтворители.

Изомеризъм на поредицата
За представители на редица парафини е характерноизомеризма на въглеродния скелет. Това се обяснява с възможността за пространствено въртене на въглеродния атом около химическите връзки. Например, за да свържете състава на C4H10, можете да вземете въглеводород с прав въглероден скелет - бутан. Тъй като структурният изомер ще бъде 2-метилпропан, който има разклонена структура.
Сред типичните химични свойства, характерниза парафините е необходимо да се отбележи реакцията на заместване. Насищането на връзките обяснява сложността на реакцията, нейния радикален механизъм. За да се получат халогенирани производни на алифатни въглеводороди, е необходимо да се проведе реакцията на халогениране, която протича в присъствието на ултравиолетова радиация. Веригата на това взаимодействие се наблюдава при всички представители на тази серия. Получените продукти се наричат халогенни производни. Те се използват широко в химическата промишленост като органични разтворители.
В допълнение, всички алифатни и ароматнивъглеводородите изгарят в присъствието на кислород, образувайки вода и въглероден диоксид. В зависимост от процентното съдържание на въглеродната молекула се отделя различно количество топлина. Независимо от принадлежността към класа на органичните съединения, всички процеси на изгаряне са екзотермични реакции, използвани в ежедневието и промишлеността.
Дехидрогенирането на метан (разцепване с водород) също има практическо приложение. В резултат на този процес се образува ацетилен, който е ценна химическа суровина.

Използването на алкани и хлорирани алкани
Дихлорметан, хлороформ, тетрахлоретан - течности,които са отлични органични разтворители. Хлороформът и йодоформът се използват в съвременната медицина. Разграждането на метан е един от индустриалните методи за производство на сажди, които са необходими за производството на печатарско мастило. Метанът се счита за основен източник на производство на газообразен водород в химическата промишленост, който се отнася до производството на амоняк, а също и до синтезата на множество органични вещества.
Ненаситени въглеводороди
Ненаситените алифатни въглеводороди сапредставители на редица етилен и ацетилен. Нека анализираме основните им свойства и приложения. Алкените се характеризират с наличието на двойна връзка, така че общата формула за серията има формата CnH2n.
Предвид ненаситения характер на тези вещества,може да се отбележи, че те влизат в реакцията на съединението: хидрогениране, халогениране, хидриране, хидрохалогениране. В допълнение, представителите на редица етилени са способни на полимеризация. Това е особената особеност, която прави представителите на този клас в търсенето в съвременното химическо производство. Полиетиленът и полипропиленът са веществата, които съставляват основата на полимерната промишленост.
Ацетиленът е първият представител на серията, която имаобщата формула CnH2n-2. Сред отличителните характеристики на тези съединения може да се установи присъствието на тройна връзка. Неговото присъствие обяснява протичането на реакциите на съединението с халогени, вода, водороден халогенид, водород. Ако тройната връзка в тези съединения се намира в първото положение, тогава за алкините е характерна качествена реакция на заместване с комплексна сребърна сол. Тази способност е качествена реакция към алкин, използвана за откриването му в смес с алкен и алкан.
Ароматните въглеводороди са циклични ненаситени съединения, поради което не се считат за алифатни съединения.

заключение
Въпреки разликите в количествения състав,съществуващи в представители на ограничаващи и ненаситени алифатни съединения, те са подобни по качество, съдържат въглерод и водород в молекулите. Различията в количествения състав (различни общи формули) в представителите на наситени и ненаситени CCI2 обясняват разликата в механизмите на реакциите при получаване на различни продукти.
Ето защо представители на всички класове такивасъединенията влизат в реакциите на горенето, образуват въглероден диоксид, вода, освобождават определено количество топлинна енергия, което ги прави търсени като гориво в ежедневието и промишлеността.

